20年ほど前まで、「抗がん剤による治療の効果はほとんどない」といわれていた。また、数年前までは、海外で承認された医薬品が日本の医療現場で使えないことが、がん治療を遅らせるとして問題視されていた。
こうしたことを1つ1つ乗り越えて、現在のがん治療がある。
「ドラッグ・ラグ」の解消に長年尽力してきた国立がん研究センター名誉総長の堀田知光医師に医薬品によるがん治療の問題点や展望について聞いた。
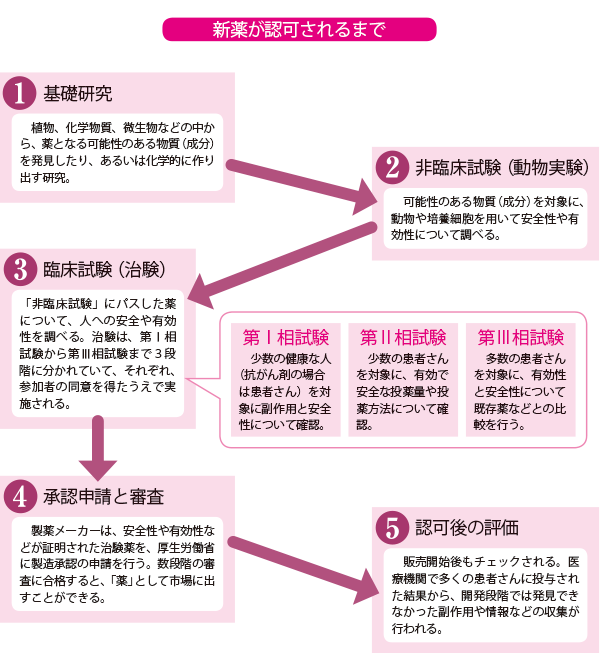
臨床研究中核病院の設置や審査員を増やすことで「ラグ」を解消
ここ数年の間に抗がん剤は進歩し、高い治療成績を上げている薬も多い。しかし、海外ではすでに承認されている抗がん剤や、諸外国の医学書に載っている薬が、日本では使えない場合がある。その原因の1つとして問題視されてきたのが、「ドラッグ・ラグ」だ。
ドラッグ・ラグにはいくつかの側面があるが、この場合は、海外ではすでに効果が証明され、承認・販売されているが、日本で承認、販売されるまでの時間の「ずれ」を指す。
日本の医療現場で使うためには、日本における試験や審査を経なければならない。現状では効果的な薬がないために新薬の承認が待たれる患者さんにとって、特にこうした時間のずれは問題だ。
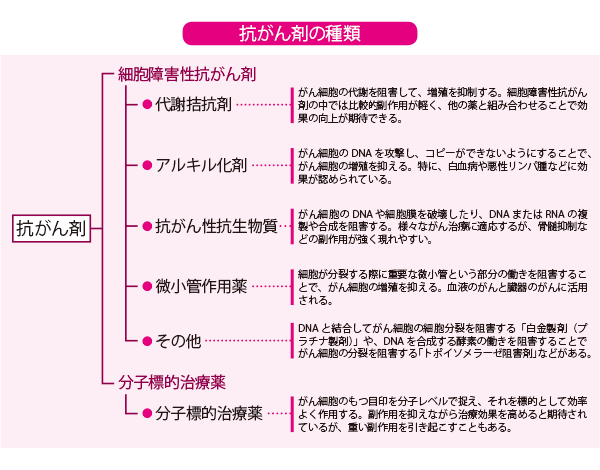
がん治療の柱には、「3大療法」と呼ばれる「外科療法」「放射線療法」「薬物療法」がある。その中の薬物療法は、抗がん剤を中心とする薬剤で行われる。抗がん剤は、今でこそ安全で有効なものが増えたが、約20年前までは治療成績が極めて低く、「抗がん剤は副作用が強いばかりで、ほとんど効かない」というのが常識だった。
これについて堀田医師は、「私が専門とする血液内科の世界でも、以前は悪性リンパ腫や白血病の患者さんに効果はあるが限定的で、その他の分野の固形がんは、ほとんど治らなかったといってもいいでしょう」と振り返る。
しかし、1980年代後半から、がんの浸潤や転移、増殖に関係する重要な分子が明らかになり、90年代後半に分子標的薬の臨床開発が始まると、抗がん剤の治療成績は向上し、この流れに乗って世界中で次々に新薬が開発されていく。そこで浮き彫りになってきたのがドラッグ・ラグの問題だった。
「数年前までは、アメリカと日本のドラッグ・ラグが4年、世界の平均と日本とでは2.5年とされていました。もちろん、安全性と有効性を厳しく審査する姿勢は大切ですが、より効果的な薬を望む大勢の患者さんのことを考えると、時間差があり過ぎるのは問題だと思います」
ドラッグ・ラグを縮めるにはどうしたらよいか――。この問題を解決するため、厚生労働省は、2005年に「未承認薬使用問題検討会議」を設置。さらに2010年には、「医療上の必要性の高い未承認薬・適応外薬検討会」に移行し、ドラッグ・ラグの解消を加速してきた。ドラッグ・ラグの問題を重視した堀田医師はこのような会議で座長を務め、積極的に問題提起や多方面への働きかけを試みて、「ミスター・ドラッグ・ラグ」と呼ばれたこともあった。
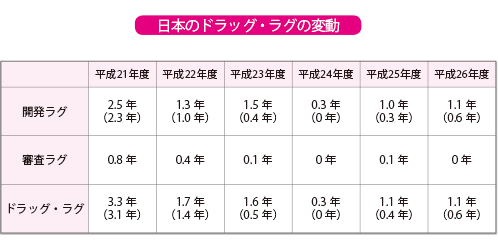
*薬事申請までの時間のずれを「開発(申請)ラグ」、薬事審査における時間のずれを「審査ラグ」と呼ぶ。ドラッグ・ラグは、開発ラグと審査ラグの和。
*カッコ内の数値は、検討会品目(厚生労働省において開催された「医療上の必要性の高い未承認薬・適応外薬検討会議」における検討の結果、申請された品目)を除いた場合の値。
(PMDAによる「ドラッグ・ラグの試算」を一部改変)
ドラッグ・ラグが長いのは、海外に比べて日本の治験や審査の基準が厳しく、時間を要するためとされていたが、治験着手段階での遅れの影響も大きかった。その理由としては、治験の環境が十分に整っていなかったことが挙げられる。「アメリカや韓国には、入院患者が5000人というような巨大規模の病院があり、そこにはあらゆる分野の専門医がそろっていますから、治験なども一気にできます。しかし、日本にはこれほどの規模の病院がなく、専門医も散らばっていますから、どこで治験をするかということから検討しなくてはならなかったのです」。
そこで厚生労働省は、専門性と臨床試験の効率化に必要な機能を備えた臨床研究中核病院を設置した。こうした病院を核にネットワーク化を進め、英語に堪能な治験コーディネーターなども育成。さらに国際共同治験に参加することで、治験にかかる時間の短縮を目指した。
また、国から薬の審査を委託された独立行政法人医薬品医療機器総合機構(PMDA)の審査員を増やすことで、審査に要する時間は、短縮されるようになった。
より新しく効果的な標準治療のために創薬国としての成長を目指す
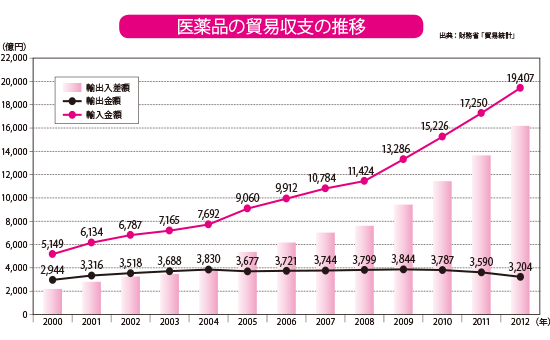
医薬品の問題はドラッグ・ラグの他にもあり、「高額過ぎる薬価」もその1つだ。抗がん剤は海外から輸入されるものも多い。上のグラフを見れば、医薬品の輸入金額が輸出金額をはるかに超えているのが分かる。
日本はアメリカやイギリスに次ぐ創薬国とされ、抗がん剤の開発も進んでいるが、アメリカとの差は大きく、例えば2010年において、アメリカの創出数が39であったのに対し、日本は13とアメリカの3分の1にとどまっている。
「創薬開発を担っているのは、主にベンチャー企業。アメリカの場合、経済面を中心にベンチャー企業を支援する仕組みが整っています。そこが日本と最も違う点といえるでしょう」。日本の創薬への取り組みは、まだ十分とはいえず、現在は、2015年に設立された日本医療研究開発機構が、基礎段階から実用化まで、一貫した研究のマネージメントを担っている。
しかし、輸入薬に限らず、国内で開発されたものの中にも高額な医薬品はある。
「基礎研究の段階で発見された医薬品の候補が、新薬として承認される可能性は、約2万2000分の1。しかも開発に要する期間は、9年から長いものでは15年にも及びます。その間にかかった費用を回収しようとすると、どうしても薬の価格は高くなります」
高額な薬でも保険適用であれば、患者さんの支払う医療費は一定額に抑えられる。だが、保険の財源が有限であることを考慮すると、治療効果が見込まれる患者さんに絞って処方する必要があり、これを見極める研究も進んでいる。
このように新薬が開発され、治療に使われるようになることで、がん種による差はあるものの、全体的に標準治療のレベルも上がってきている。
「標準治療をスタンダードな『並みの治療』と捉えている人が多いようですが、安全性の証明された『現状で最もすぐれた治療』というのが正しい解釈です。しかも、どこの病院でも同じように受けられる治療。これに対して先進医療は、その名称から最新の治療とイメージしがちですが、こちらはまだ評価中の未確定な治療法です。この区別は、治療中のがん患者さんにもご家族にも、正しく知っておいてほしいですね」
3大療法に緩和ケアや免疫療法などを組み合わせた集学的治療で効果を高めようとする考え方も主流になりつつある。創薬に力を入れ、新たな治療法を創り出そうとする動きは、今後ますます活発になっていくだろう。
 堀田 知光
堀田 知光
国立がん研究センター名誉総長/国立病院機構名古屋医療センター名誉院長
ほった・ともみつ●1969年、名古屋大学医学部を卒業後、東海大学医学部長を経て、2006年、国立病院機構名古屋医療センター院長に就任。12年には国立がん研究センター理事長に。現在は両センターの名誉総長、名誉院長を務める。専門分野は血液内科。日本血液学会名誉会員、厚生労働省「がん対策推進協議会」委員など歴任。
(取材時現在)

