日本で生まれた新しいタイプの抗がん剤、免疫チェックポイント阻害薬が注目を集めています。抗PD-1抗体薬オプジーボなど免疫チェックポイント阻害薬ががんを治す仕組み、その効果や副作用、今後の課題などについて、がん免疫療法の専門家である吉村先生に解説いただきます。
T細胞の働きにブレーキをかけて自分の身を守るがん細胞
私たちの体の中では毎日数千個のがん細胞が生まれているとされる。それをことごとく見つけては殺してくれるのが免疫細胞だ。この免疫細胞のおかげで私たちはがんにならないですんでいる。
ところが、ときに免疫細胞の監視の目をかいくぐるがん細胞がいて、これが年月をかけて大きく成長、私たちの命を脅かす。このため、従来のがん免疫療法では、免疫細胞の数を増やしたり、活性化させたりして、がんを退治しようとしてきた。
しかし、最近、がん細胞のほうでも何やら細工をしていることに研究者たちが気付いた。実はがん細胞は自分の身を守るために、「免疫チェックポイント」という裏技を使い、免疫細胞を無力化していたことが分かったのだ。
国立がん研究センターの吉村清免疫療法開発分野長は、免疫チェックポイントについて、こう説明する。
「免疫の主役ともいえるT細胞ですが、常に活性化している状態が望ましいわけではありません。免疫の働きが暴走すると、自分自身の体を攻撃して、関節リウマチのような自己免疫疾患を引き起こすからです。そのためT細胞には免疫を活性化するだけでなく、過剰反応を起こさないように抑制する機能も備わっています。自動車にアクセルとブレーキがあるようなもので、ブレーキに当たるのが、免疫チェックポイントです」
T細胞は、細菌やウイルスなどの異物が体内に入ってくると、樹状細胞のようにそれを知らせる抗原提示細胞を通じて、異物の情報を得る。このとき樹状細胞は司令塔の役目を果たし、T細胞を活性化したり、働きを抑えたりして、コントロールしようとするが、がん細胞は、このT細胞の働きを抑える機構を巧みに模倣しようとするのだ。抑制の信号を送るための樹状細胞のアンテナ(リガンドという)と同じアンテナをがん細胞が出すのである。がん細胞が出した抑制信号を受け取ったT細胞の働きにはブレーキがかかってしまう。この機構が、免疫チェックポイントの本性である。
T細胞の受容体で免疫チェックポイントに関係するものには、PD-1、CTLA-4などがある。一方、これに合致するリガンドでがん細胞にも発現しているものにはPD-L1があり、このPD-L1がPD-1にT細胞が働かないように信号を送る。
免疫チェックポイント阻害薬は、免疫のはたらきを復活させる薬
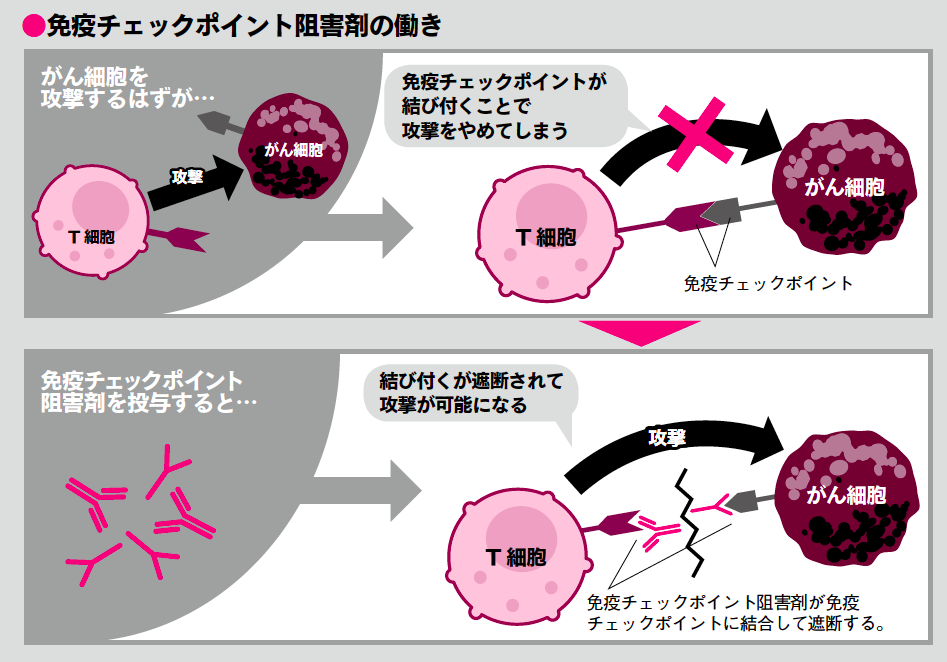
吉村分野長は、T細胞のブレーキのスイッチが入らないようにT細胞とがん細胞が結合するのを阻害する薬、「免疫チェックポイント阻害薬」(上図参照)の研究を進めている。
現在、日本で治療に使われている免疫チェックポイント阻害薬には、抗PD-1抗体のニボルマブ(商品名オプジーボ)と抗CTLA-4抗体のイピリムマブ(商品名ヤーボイ)の2つがある(※)。
日本では、根治切除不能な悪性黒色腫にニボルマブ(オプジーボ)とイピリムマブ(ヤーボイ)が、切除不能な進行・再発の非小細胞肺がんにニボルマブが承認されている。他社の抗PD-1抗体や、抗LAG-3抗体、抗PD-L1抗体、抗OX40抗体などが各国で治験段階にある。転移して打つ手がなくなったがん患者さんに長期生存が可能な薬が登場して世界中の期待を集めている。
免疫チェックポント阻害薬は、現時点では一定のがん種にのみ有効とされ、どのようながん種に有効かは、各国で研究が進められている。この薬剤の大きな特徴の1つに、従来の治療に比べ、副作用の頻度が少ない点が挙げられる。しかし、ときには、I型糖尿病や間質性肺炎などの重篤(じゅうとく)な副作用を起こすこともあるので注意が必要だ。
※オプジーボ®、ヤーボイ®はブリストル・マイヤーズ スクイブ社の登録商標です。
日本で生まれた免疫チェックポイント阻害薬
免疫チェックポイント阻害薬は日本で生まれたまったく新しいタイプの抗がん剤。受容体の発見から実用化まで中心的な役割を果たしてきたのが京都大学の本庶佑博士だ。ノーベル賞の有力候補でもある。
1992年、本庶博士の研究グループが免疫細胞にアポトーシス(細胞死)を起こす分子を探すなかでPD−1を発見した。その後、本庶博士はマウスを使った実験でPD−1が活性化した免疫細胞の働きを抑制することを証明。99年に論文に発表した。この発見が画期的ながん治療薬につながると考えた本庶博士は、製薬会社などと共同で抗がん剤の開発に着手。2014年、抗PD−1抗体の免疫チェックポイント阻害剤「ニボルマブ」の商品化に成功した。
なお、米国でも別の免疫チェックポイント分子「CTLA−4」が発見され、2011年には抗CTLA−4抗体の「イピリムマブ」が発売されている。
もう1つの特徴は、効果がある人には、その効き目が長持ちするという点だ。
例えば、進行性の悪性黒色腫の患者さんの約2割が10年を超えて生存しているとのデータもある。免疫チェックポイント阻害剤は直接がん細胞を攻撃するものではなく、T細胞に働きかけてがんをたたく薬のため、耐性の問題が起こりにくいと考えられる。
ただし吉村分野長は「肺腺がんで、しばらくすると生存率が落ちたデータもあり、すべてのがん種で長く効くわけではない」と指摘する。
課題は薬価の高さやタイプ別奏効率の解明
今後の課題としては、薬価が高い点をどうするかということが挙げられる。体重60キロの患者さんに2週間ごとに投与すると、1カ月約260万円かかるという。
保険が適用されるため、患者さんの負担はそれほど重くはないが、今後、適応範囲が広がれば、国の保険財政がもたなくなりそうだ。
また、薬価が高いだけに免疫チェックポイント阻害薬が効く人と効かない人をどう見分けるかという問題もある。ニボルマブを例に取ると、患者さんのがん細胞のPD-L1の発現量を調べれば、効果のあるなしが予測できそうだが、発現量と治療効果に関係性は見られないという。
個々の薬に対する効き方を事前に予測できるバイオマーカーの探索に関しては、各国で熱心な研究が進められている。
米国からの報告によると、大腸がんの場合、遺伝子検査を行った結果、特に遺伝子変異の著しいタイプの大腸がんによく効いたという。これを裏付けるものとして、遺伝子の変異が起こりやすいがんのほうが異物として認識しやすいので、免疫が働きやすくT細胞が集まりやすいというデータがある。
だが、必ずしもこの理論が当てはまらない場合もあり、免疫チェックポイント阻害剤を使った治療効果の予測には、様々な角度からアプローチが行われている。
免疫細胞治療などとの併用に期待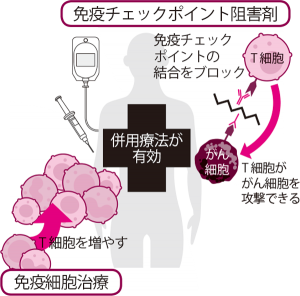
免疫チェックポイント阻害薬は、それ自体にがんを殺傷する力はない。免疫のブレーキを解除するだけで、あとは体が元々もっている免疫の力で、がんが治ることを証明した点で画期的といえる。
ただ、免疫チェックポイント阻害剤単独での奏効率は2~3割といわれる。これは、そもそもがん患者さんでは健康な人に比べて、攻撃する免疫が十分に機能していないことも一因と考えられる。このことから、患者さんの免疫細胞を体外で活性化させて体に戻す「免疫細胞治療」と組み合わせれば大きな効果が得られるのではと期待されている。ただし免疫チェックポイント阻害剤は、実際の治療で使われるようになってからまだ日が浅い。そのため、今後期待される併用療法を安全に、効果的に行うためにも、慎重に研究を進める必要があるだろう。


